sur SANOFI-AVENTIS (EPA:SAN)
Dupixent de Sanofi et Regeneron recommandé pour une autorisation de mise sur le marché dans l'UE pour le traitement de l'urticaire chronique spontanée chez l'enfant
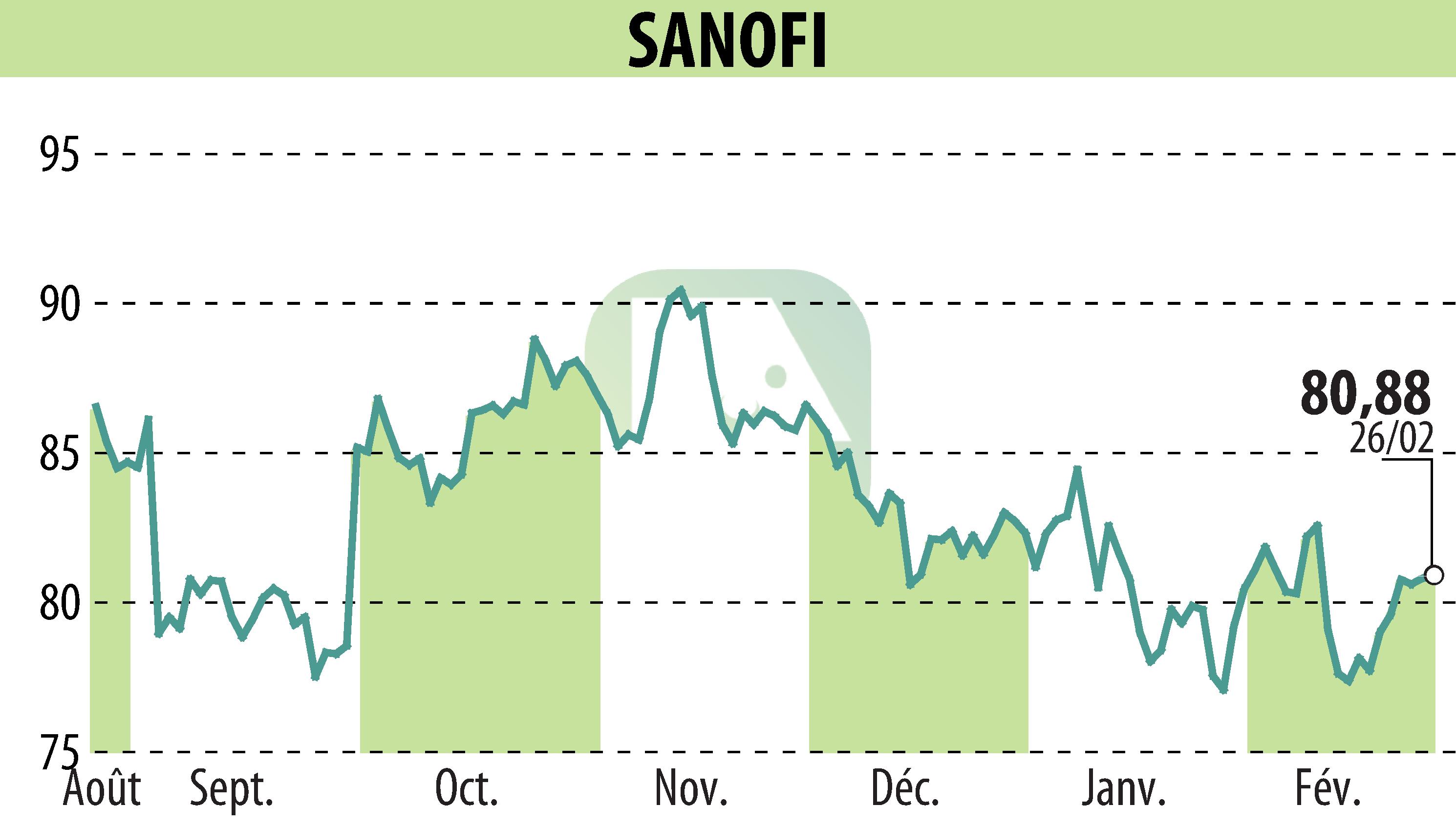
Sanofi et Regeneron ont annoncé que le Comité des médicaments à usage humain (CHMP) de l'Agence européenne des médicaments (EMA) a émis un avis favorable concernant Dupixent (dupilumab) pour le traitement de l'urticaire chronique spontanée (UCS) chez les enfants âgés de 2 à 11 ans. S'il est approuvé, Dupixent serait le premier médicament ciblé dans l'UE pour les enfants atteints d'UCS insuffisamment soulagée par les antihistaminiques. Cette affection est connue pour provoquer des crises d'urticaire et des démangeaisons invalidantes dues à une inflammation de type 2, altérant la qualité de vie des enfants.
Cette recommandation repose sur le programme clinique LIBERTY-CUPID, qui comprenait des études menées auprès de participants âgés de six à onze ans, ainsi qu'une étude portant sur des enfants âgés de deux à onze ans. Dupixent est déjà autorisé pour le traitement de l'urticaire chronique spontanée (UCS) chez l'adulte et l'adolescent aux États-Unis, dans l'Union européenne et au Japon. La Commission européenne se prononce actuellement et la FDA américaine devrait rendre sa décision d'ici avril 2026. Sanofi et Regeneron poursuivent leurs recherches sur le potentiel de Dupixent dans d'autres maladies inflammatoires.
R. P.
Copyright © 2026 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de SANOFI-AVENTIS
