sur GENSIGHT BIOLOGICS S.A. (EPA:SIGHT)
GenSight Biologics : Point sur les Programmes d'Accès Précoce et l'Étude REVISE
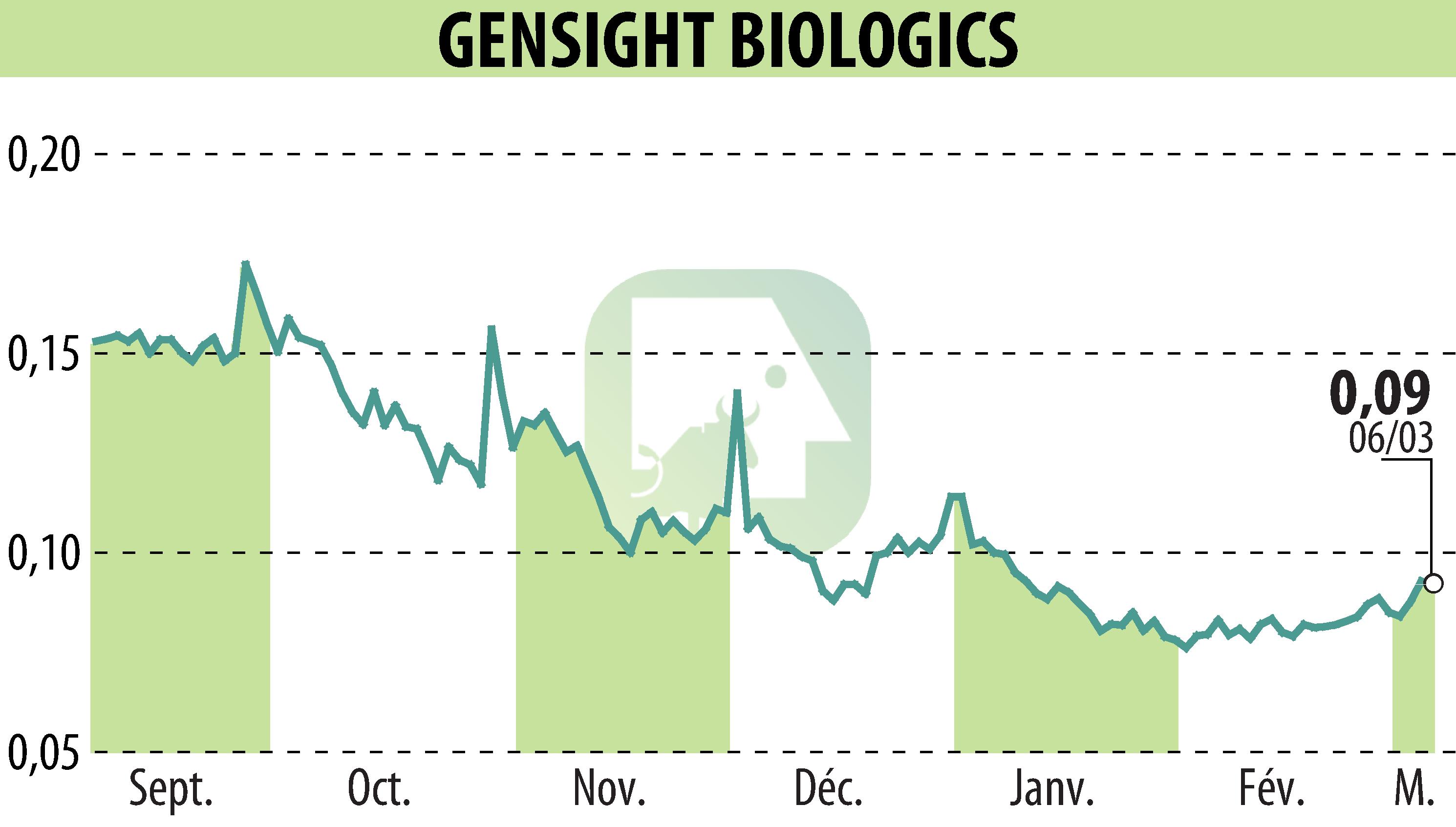
GenSight Biologics, société biopharmaceutique en phase clinique, fournit une mise à jour sur ses programmes d'accès précoce pour GS010/LUMEVOQ® et l'étude REVISE. GS010/LUMEVOQ®, thérapie génique en développement pour la Neuropathie Optique Héréditaire de Leber, poursuit son avancée en France, Israël et aux États-Unis.
En France, após approbation de l'Autorisation d'Accès Compassionnel par l'ANSM, les traitements débuteront en mars à l'Hôpital des 15-20. L'étude REVISE suit son calendrier avec un patient traité et un second bientôt recruté.
Israël a approuvé le traitement d'un deuxième patient via le programme payant d'accès précoce, et aux États-Unis, l'autorisation d'une seconde demande d'IND individuelle par la FDA permettra un nouveau traitement dans le cadre du programme "Expanded Access".
Les recettes attendues sont jugées suffisantes pour maintenir les opérations de la société en 2026.
R. E.
Copyright © 2026 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de GENSIGHT BIOLOGICS S.A.
